إختيار جنس الجنين
من جيلٍ إلى جيل، يَتناقلُ الناس طُرقًا للتحكم في جنس الجنين. مُعظم هذه الطُرق لا أساس لها من الصحة أَوْ لا يُوجد أدلة علمية كافية لدعمها.
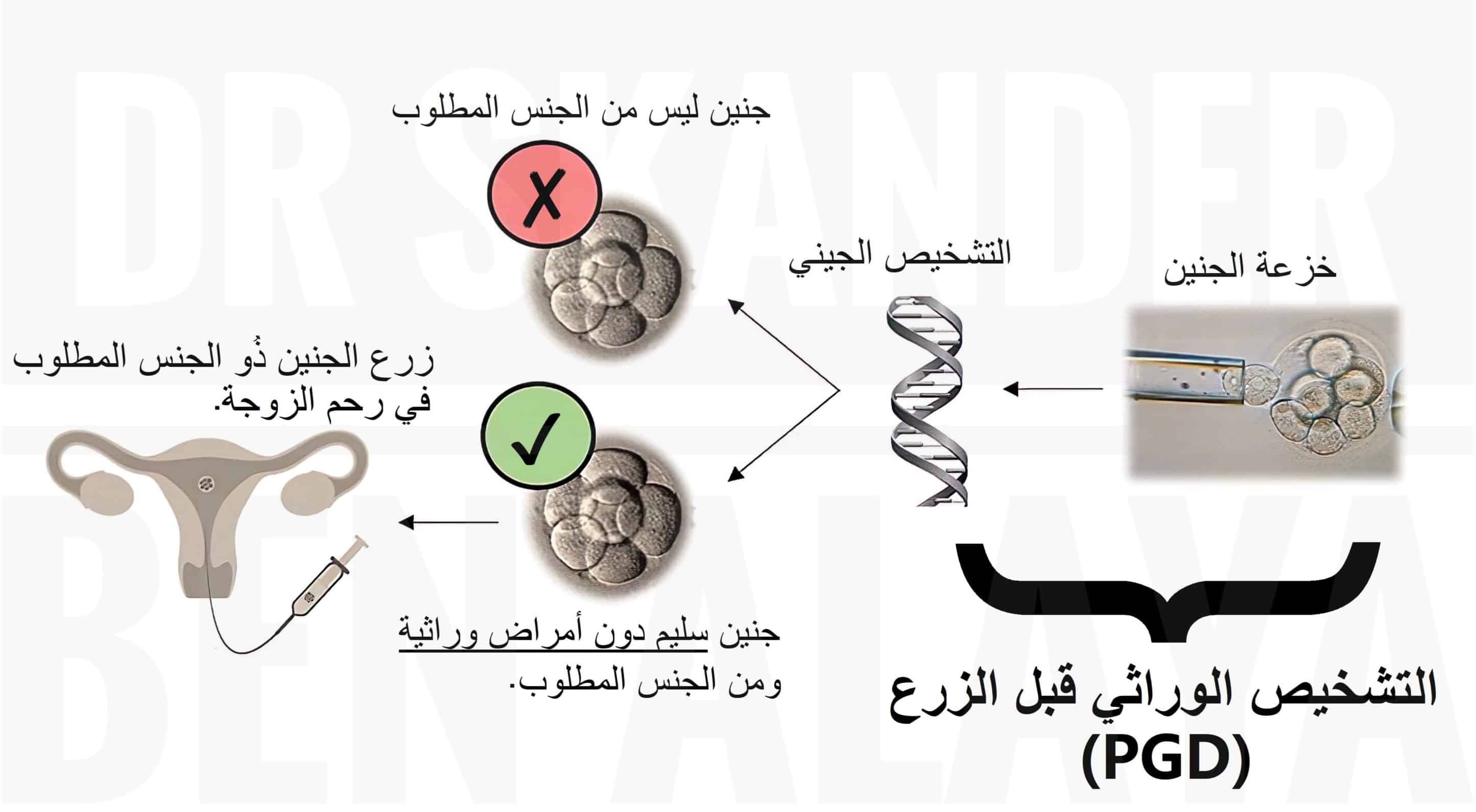
لإختيار جنس الجنين، يقومُ الأطباء أَوَّلاً بتحديد جنس الأجنة من خلال تقنية التشخيص الوراثي قبل الزرع (PGD). بعد ذلك، يتم زرع الجنين ذُو الجنس المطلوب في رحم الزوجة.
هُناك إمكانيّة طبيّة أُخرى، وهي فصل الحيوانات المنوية الذكرية عن الأنثوية ثُمَّ إستخدام العينة الغنية بالحيوانات المنوية المطلوبة في عمليات التلقيح. تُوجد عِدَّة طُرق لفرز الحيوانات المنوية، لكِنَّ MicroSort أكثرها دقة وفعَّالية.
إتصل بالدكتور إسكندر بن علية عبر الهاتف، واتساب أو فايبر
فرز الحيوانات المنوية (Sperm sorting)
الجنين ناتج من إتحاد حيوان منوي قد يحمل الكروموسوم (X) أو (Y)، مع بويضة تحمل دائمًا الكروموسوم (X).
- إذا لُقِّحت البويضة بحيوان منوي يحمل كروموسوم الأنوثة (X)، يَكُون الجنين أُنثى (XX).
- إذا لُقِّحت البويضة بحيوان منوي يحمل كروموسوم الذكورة (Y)، يَكُون الجنين ذكرًا (XY).
تَعتمِدُ طُرُق فرز الحيوانات المنوية على فصل الحيوانات المنوية التي تحمل الكروموسوم (X) عن تلك التي تحمل الكروموسوم (Y). يحتوي الحيوان المنوي الأنثوي على نسبة من الحمض النووي (DNA) تزيد ب 2.8% عن الحيوان المنوي الذكري. بناءً على ذلك، يُمكن لِ MicroSort تحديد الحيوان المنوي الذي يحمل الكروموسوم الأنثوي (X) وتفريقه عن الحيوان المنوي الذي يحمل كروموسوم الذكورة (Y).
تبدأ طريقة MicroSort بغسل الحيوانات المنوية لإزالة الشوائب والحيوانات المنوية غير المتحركة. بعد ذلك، يقوم أخصائي التحاليل الطبية بإضافة صبغة فلورية خاصة ترتبط بالحمض النووي داخل خلية الحيوان المنوي. لإحتوائه على نسبة أعلى من المادة الوراثية، يَمتصُّ الحيوان المنوي الأنثوي كمية أكبر من الصبغة مقارنة بنظيره الذكري. نتيجةً لذلك، عند التَعرُّض لشعاع الليزر أثناء قياس التدفق الخلوي، يُصدر الحيوان المنوي الأنثوي إشارة فلورية أقوى من نظيره الذكري. يستخدم جهاز مقياس التدفق الخلوي (Flow Cytometer) برنامج حاسوب لتحديد الحيوانات المنوية (X) و(Y) بناءً على شدة الإشارة الفلورية المنبعثة من كل حيوان منوي.
يتم فرز الحيوانات المنوية إلى مجموعتين: مجموعة تحمل الكروموسوم X (لإنجاب الإناث)، ومجموعة تحمل الكروموسوم Y (لإنجاب الذكور). في مرحلة أخيرة، يتم إستخدام الحيوانات المنوية التي يختارها الزوجان في عمليات التلقيح الإصطناعي داخل الرحم، طفل الأنبوب أو الحقن المجهري لتحقيق الحمل بالجنس المطلوب.
سَجَّلت طريقة MicroSort نِسَب نجاح تصل إلى 90% عند إختيار الحمل بجنين أنثى و70-80% عندما يكون الهدف هو الحمل بجنين ذكر. طريقة MicroSort غير مُرخَّصة من قبل إدارة الغذاء والدواء الأميركية (FDA). لا تَتوفَّرُ هذه الطريقة إلاَّ في المكسيك، ماليزيا، اليابان، شمال قبرص، كمبوديا، تايلاندا ونيجيريا.
تحديد جنس الجنين بإستخدام التشخيص الوراثي قبل الزرع (PGD)
يُستخدم التشخيص الوراثي للأجنة (PGD) كجزء من عمليات طفل الأنبوب والحقن المجهري، ويُوفِّرُ مسحًا جينِيًّا مُبكِّرًا للجنين قبل زرعه في الرحم. يلجأ الأزواج إلى التشخيص الوراثي للأجنة (PGD) للحمل بجنين صحي خالٍ من الأمراض الوراثية. أثناء دراسة الخلايا الجنينِيَّة، يُمكن للطبيب تحديد (مَعرِفَة) جنس الجنين بدقة تصل إلى 99%.
تُعدُّ الخزعة الجنينية (Biopsy) إحدى الخطوات الأساسية في إختبارات التشخيص الوراثي قبل الزرع، حيث يتم أخذ عينة من خلايا الجنين لتحليل المادة الوراثية والكشف عن أي إضطرابات جينية أو صبغية قبل نقل الجنين إلى الرحم. تُجرى خزعة الجنين في مرحلتين رئيسيتين: اليوم الثالث بعد الإخصاب (مرحلة الإنقسام – Cleavage Stage)، أو اليوم الخامس بعد الإخصاب (مرحلة الكيسة الأريمية – Blastocyst Stage). بعد الحصول على العينة، تُستخدم تقنيات متقدمة (التهجين الموضعي المتألق، التهجين الجيني المقارن، تسلسل الجيل التالي، تسلسل الجيل الثالث، وتسلسل الجيل الرابع) لتحليل الجينوم، والكشف عن الإضطرابات الوراثية، وتحديد جنس الجنين. يَكُون إختيار التقنية التي سَتُدرَسُ بها الخلايا الجنينية وفقًا للمُشكلة الوراثية التي سيتم التحقيق فيها.
التهجين الموضعي المتألق (FISH)
يعتمد التهجين الموضعي المتألق على إستخدام المجسات الفلورية لإستهداف مناطق معينة من الكروموسومات مباشرة داخل الخلايا المستخلصة من الجنين، مِمَّا يسمح بفحص الجنس وعدد محدود من الكروموسومات تحت المجهر الفلوري.
في اليوم الثالث بعد الإخصاب (مرحلة الإنقسام – Cleavage Stage)، يتم أخذ 1-2 خلية من الجنين المكوَّن من حوالي 8 خلايا. تُجرى الخزعة عبر عمل ثقب دقيق بالليزر في المنطقة الشفافة (Zona Pellucida) المحيطة بالجنين. يتم وضع الخلايا على شريحة زجاجية خاصة، وتُثبَّت بإستخدام محاليل كيميائية (Fixation) للحفاظ على بنية الكروموسومات. تُضاف المجسات الفلورية إلى العينة وتُترك للإرتباط بالمواقع المستهدفة على الكروموسومات. يتم غسل العينة لإزالة المجسات غير المرتبطة. يُستخدم مجهر فلوري لرؤية الإشارات الفلورية وتحديد:
- جنس الجنين.
- عدد الكروموسومات للكشف عن الإختلالات العددية (مثل التثلث الصبغي – Trisomy).
- حذف أو تكرار مناطق جينية محددة في الكروموسومات.
التهجين الموضعي المتألق (FISH) هو تقنية بسيطة ومحدودة مقارنة بالتقنيات الجينية الأخرى، ولا يتطلب تحضيرات معقدة، فهو لا يحتاج إلى تضخيم الحمض النووي، لأنَّه يعتمد على الكشف المباشر داخل الخلايا. لا يحتاج إلى تقطيع الحمض النووي، لأنَّه يتم إجراء التهجين داخل الخلايا المثبتة دون الحاجة إلى تكسير الحمض النووي أو تحضيره بشكل خاص. لا يتطلب قراءة تسلسل الـ DNA بالكامل، بل يُركِّز على المناطق المُستهدفة مسبقًا مُعتمِدًا على إشارات فلورية مرئية فقط. لا يحتاج إلى تجميع البيانات الجينية، لأنَّ التحليل يتم بصريًّا بالمجهر الفلوري (لا يتم التعامل مع بيانات رقمية معقدة).
إختبار التهجين الموضعي المتألق (FISH) يستغرق عادة 24 إلى 48 ساعة للحصول على النتائج، مِمَّا يسمح بنقل الأجنة السليمة وراثيا ومن الجنس المطلوب في نفس الدورة العلاجية (Fresh Embryo Transfer) دون الحاجة إلى تجميدها. إذا كانت هناك حاجة لفحص شامل لجميع الكروموسومات أو الأمراض الوراثية، يتم اللجوء إلى تقنيات أخرى أكثر دقة من FISH، رغم أنَّها تتطلَّب وقتًا أطول، مِمَّا قد يستوجب تجميد الأجنة.
ملاحظة: يُمكن تطبيق تقنية التهجين الموضعي المتألق (FISH) أيضًا على أجنة الكيسة الأريمية في اليوم الخامس بعد الإخصاب.
التهجين الجيني المقارن (CGH array)
التهجين الجيني المقارن أكثر شمولية من FISH، فهو يُوفّرُ مسحًا شاملاً لِكُلِّ كروموسومات الجنين، بما في ذلك الكروموسومات الجنسية. تعمل تقنية CGH array على مقارنة الحمض النووي الجنيني مع حمض نووي مرجعي طبيعي للكشف عن أي إختلافات كمية دون الحاجة إلى معرفة مسبقة بالمناطق المتأثرة.
في اليوم الخامس، يتطور الجنين إلى مرحلة الكيسة الأريمية، يتم أخذ 5-10 خلايا من الطبقة الخارجية للجنين (الأرومة الغاذية – Trophectoderm)، والتي ستصبح لاحقًا المشيمة، دون التأثير على الكتلة الخلوية الداخلية التي ستتطور إلى الجنين. تُستخدم تقنيات كيميائية أو إنزيمية لإستخلاص الحمض النووي من الخلايا المأخوذة من الجنين. تُستخدم تقنية تضخيم الجينوم بالكامل (WGA) لتكبير كمية الحمض النووي القليلة المُستخرجة من الخلايا.
لتمييز الحمض النووي الجنيني عن المرجعي أثناء التهجين، يُلوَّنُ الحمض النووي الجنيني بصبغة فلورية (مثل الأخضر)، ويُلوَّنُ الحمض النووي المرجعي بصبغة فلورية مختلفة (مثل الأحمر). لتسهيل عملية التهجين عن طريق تقليل طول قطع الـ DNA، يتم تكسير الحمض النووي إلى قطع صغيرة بإستخدام تقنيات مثل الإنزيمات المقيدة (Restriction Enzymes) أو الموجات فوق الصوتية. يتم خلط الحمض النووي الجنيني والمرجعي المُلوَّنين معًا، ثم تُوضع العينة على شريحة زجاجية تحتوي على آلاف المجسات (Probes) الموزعة على جميع مناطق الجينوم. تُترك العينة لمدة 16-24 ساعة في درجة حرارة مُحكمة للسماح للحمض النووي بالإرتباط بالمجسات.
بعد التهجين، يتم غسل الشريحة لإزالة أي DNA غير مرتبط. يتم إستخدام ماسح ضوئي فلوري (Fluorescence Scanner) للكشف عن الإشارات الفلورية لكل موقع على الشريحة. تُقاس شدة الإشارات الفلورية لكل لون (الأخضر والأحمر) في كل منطقة من الجينوم. تُحسب نسبة الإشارتين (الأخضر/الأحمر) لتحديد ما إذا كان هناك زيادة أو نقصان في المادة الوراثية في الحمض النووي الجنيني مقارنةً بالمرجعي. تُستخدم برامج حاسوبية متخصصة لتحويل الإشارات الفلورية إلى بيانات رقمية. يُحدِّد التقرير النهائي الأجنة السليمة جينيًّا ومن الجنس المطلوب لنقلها إلى الرحم.
يتم تجميد الأجنة مؤقتا بعد الخزعة مباشرةً وذلك لأنَّ التهجين الجيني المقارن (CGH array) عادةً ما يستغرق ما بين 3 إلى 5 أيام للحصول على النتائج. يتم النقل لاحقًا في دورة أخرى.
تسلسل الجيل التالي (NGS)
في تسلسل الجيل التالي، تُجرى الخزعة في اليوم الخامس بعد الإخصاب، أي عند وصول الجنين إلى مرحلة الكيسة الأريمية. يتم إستخراج الحمض النووي (DNA) من الخلايا المأخوذة من الجنين، وهي كمية صغيرة جدًّا تتطلب تضخيمًا بإستخدام تقنية (WGA)، مِمَّا يسمح بالحصول على كمية كافية للتحليل الجيني. بإستخدام إنزيمات تقطيع الحمض النووي أو بطرق كيميائية أخرى، يتم يتقطيع الحمض النووي إلى أجزاء قصيرة جدًا، وذلك لتحضيره للتسلسل الدقيق. يُستخدم نظام (Massively Parallel Sequencing – MPS) لقراءة ملايين الأجزاء القصيرة من الحمض النووي بشكل متوازي. بعد قراءة التسلسل، تُستخدم خوارزميات متخصصة لتجميع الأجزاء المتسلسلة وتحليلها.
تُقارَنُ نتائج التسلسل الجيني بالجينوم المرجعي البشري للكشف عن أي تغييرات غير طبيعية. تكشف تقنية NGS الطفرات الجينية الصغيرة التي قد لا تُكتَشَفُ بإستخدام تقنيات أخرى مثل FISH أو CGH array. يتم تجميد الأجنة بعد الخزعة مباشرة لإنتظار نتائج الإختبار التي تستغرق عادةً ما بين 5 إلى 7 أيام بعد سحب خلايا الجنين. يتم نقل الأجنة السليمة وراثيا ومن الجنس المطلوب في دورة لاحقة.
تسلسل الجيل الثالث (TGS)
تعتمد تقنية تسلسل الجيل الثالث (TGS) على إستخلاص الحمض النووي من الخلايا وتجزئته قبل التحليل، وتتميز بقدرتها على قراءة تسلسلات طويلة من الحمض النووي (long-read sequencing) دون الحاجة إلى تضخيم مسبق (مثل تقنية Oxford Nanopore)، مِمَّا يسمح بتحليل المناطق الجينية المعقدة مثل التكرارات أو الإنتقالات الكروموسومية.
هناك تقنيتان رئيسيتان مستخدمتان في تسلسل الجيل الثالث: الأولى تقنية تسلسل جزيء واحد في الوقت الحقيقي (PacBio SMRT) والثانية تقنية تسلسل النانوبور (Oxford Nanopore). يتم أخذ عينة من الجنين عبر خزعة جينية في اليوم الخامس عند مرحلة الكيسة الأريمية. توفر Nanopore نتائج أسرع (قد تستغرق من 24 إلى 72 ساعة)، بينما توفر SMRT دقة أعلى (قد تستغرق من 3 إلى 5 أيام). مثل NGS، من الضروري تجميد الأجنة لحين صدور النتائج، ثم يتم نقل جنين (أو أكثر) سليم جينيًّا ومن الجنس المطلوب إلى رحم الزوجة في دورة لاحقة.
تسلسل الجيل الرابع (FGS)
تُعدُّ تقنية تسلسل الجيل الرابع أحدث التطورات في مجال التحليل الجيني، حيث تهدف إلى تحقيق تسلسل جيني فوري (Real-Time Sequencing) مع دقة أعلى وسرعة غير مسبوقة مقارنةً بتقنيات الأجيال السابقة مثل NGS (الجيل التالي) وTGS (الجيل الثالث).
يعتمد تسلسل الجيل الرابع على إستراتيجيات جديدة مثل:
- على عكس تقنيات الجيل الثالث (TGS) التي تتطلب إستخراج الحمض النووي وتجزئته، يُمكن لـ FGS إجراء التسلسل داخل الخلية مباشرةً (in situ sequencing)، مِمَّا يساعد في الحفاظ على البنية الأصلية ثلاثية الأبعاد للجينوم ودراسة التنظيم الجيني الطبيعي.
- تعتمد تقنية FGS على مجسات نانوية وكهروكيميائية للكشف عن تسلسل الحمض النووي بطريقة مباشرة، دون الحاجة إلى خطوات كيميائية معقدة مثل التضخيم أو التسمية الفلورية.
- تستخدم FGS خوارزميات الذكاء الإصطناعي والتعلم الآلي في تحليل البيانات الجينية، مِمَّا يزيد من دقة التسلسل وتقليل الأخطاء الناتجة عن الضوضاء أو التشويش في الإشارات.
لا تزال هذه التقنية في مراحل التطوير والتجريب (لم يتم بعد تطبيقها على نطاق واسع في التشخيص الوراثي قبل الزرع). يُستخدم الجيل الرابع مع خزعة اليوم الخامس، ويهدف إلى توفير نتائج سريعة جدًّا (<24 ساعة). ومع ذلك، تجميد الأجنة إجراء ضروري أثناء إنتظار نتائج FGS لضمان سلامة الأجنة وإستمرارية العمل دون ضغوط زمنية. يتم نقل الأجنة السليمة جينيا ومن الجنس المطلوب في دورة لاحقة.
يَمنعُ القانون التونسي إختيار جنس الجنين إلاَّ إذا كان الهدف مِنهُ تَفادِي إنتقال أمراض وراثية مُعيَّنة تُصيب جنسًا دون الآخر. مثلاً، يُؤثِّر مرض ضُمور العضلات على الذكور فقط. إذا كان أحد الوالدين حاملاً لهذا المرض، يتم زرع الأجنة المؤنثة فقط.
للمزيد من المعلومات حول تحديد وإختيار جنس الجنين، يُمكن التواصل مباشرة مع الدكتور إسكندر بن علية عبر الجوال، فايبر أو واتساب.
إقرأ أيضاً: الحقن المجهري الفسيولوجي – موقع واب الدكتور إسكندر بن علية.

